“隔空取物”一直以來(lái)是人類(lèi)的夢(mèng)想,這種科幻超能力現被超聲科技實(shí)現并可望用于治病救人。近日,中國科學(xué)院深圳先進(jìn)技術(shù)研究院鄭海榮研究員團隊開(kāi)發(fā)出一種相控陣全息聲鑷操控技術(shù),在生物體及血流中成功實(shí)現了對含氣囊細菌群的無(wú)創(chuàng )精準操控和高效富集,在動(dòng)物模型中實(shí)現了腫瘤靶向治療應用。相關(guān)成果以“In-vivo programmable acoustic manipulation of genetically engineered bacteria”為題發(fā)表在《自然》子刊Nature Communications期刊上。該相控陣全息聲鑷系統基于高密度面陣列換能器產(chǎn)生可調諧三維體聲波,通過(guò)對空間聲場(chǎng)在活體血管內等復雜環(huán)境中的時(shí)空精準調控,在活體血管內等復雜環(huán)境中成功操控了含氣囊細菌團簇,使其精準地移動(dòng)到目標區域并發(fā)揮治療功能,有望為腫瘤的靶向給藥和細胞治療等提供一種理想手段。

文章上線(xiàn)截圖
光、聲、電、磁等經(jīng)典物理手段是實(shí)現“隔空取物”非接觸操控物體的可能途徑。光鑷操控技術(shù)于2018年獲諾貝爾物理學(xué)獎,在微納尺度顆粒操控上展示出精準優(yōu)勢,但存在對非透明生物體穿透深度有限的問(wèn)題;磁鑷一般需要磁性顆粒的結合,易導致細胞活性受影響。相較而言,基于高頻聲波梯度聲場(chǎng)設計的聲鑷技術(shù)是一種通過(guò)聲波與目標物體相互作用產(chǎn)生輻射力以實(shí)現非接觸操控物體的方法,在非透明生物體系中具有作用力大、穿透性強、操控通量高等獨特優(yōu)勢。基于空間體波的相控陣全息聲鑷具有聲場(chǎng)時(shí)空動(dòng)態(tài)調控能力且實(shí)驗架構靈活,是生物體等復雜環(huán)境內實(shí)現對目標進(jìn)行靶向操控的理想手段。
鄭海榮研究員帶領(lǐng)深圳先進(jìn)院醫學(xué)成像團隊經(jīng)過(guò)十多年聲操控技術(shù)積累,基于超聲輻射力作用原理,利用高密度二維平面陣列和多通道可編程電子系統,結合空間聲場(chǎng)調制、超聲成像和時(shí)間反演算法,提出并構建了可編程相控陣全息聲鑷理論、技術(shù)和儀器體系,為生物體等復雜環(huán)境下的精準聲操控奠定了基礎(如圖1)。團隊分析了不同聲對比系數粒子受到的聲輻射力,完成了初步的理論驗證;模擬活體組織環(huán)境,利用時(shí)間反演矯正聲波畸變,構建復雜環(huán)境中精準聲操控的模型;交替發(fā)射超聲成像與操控脈沖,實(shí)現了非透明介質(zhì)中超聲成像實(shí)時(shí)引導的三維聲鑷。團隊繼續在相控陣全息聲鑷領(lǐng)域深耕,推動(dòng)了二維高密度超聲陣列的微型化,融合顯微成像,初步實(shí)現了細胞、微生物等的離體三維聲操控驗證,進(jìn)一步結合基因編輯等技術(shù),著(zhù)力推動(dòng)可編程相控陣全息聲鑷在各領(lǐng)域的關(guān)鍵應用。這一次,團隊推動(dòng)相控陣全息聲鑷高精度高通量操控技術(shù)取得了生物醫學(xué)應用的突破,率先實(shí)現了在體聲操控細菌對于實(shí)體腫瘤的靶向治療(如圖2)。
從理論研究層面,研究團隊提出了復雜聲場(chǎng)環(huán)境中聲輻射力離散表達與計算理論,解決了復雜聲場(chǎng)的任意結構微粒受力量化表征的瓶頸問(wèn)題,并探究了復雜環(huán)境中空間聲場(chǎng)作用下操控目標的動(dòng)力學(xué)行為。從工程研發(fā)層面,團隊成員馬騰研究員等通過(guò)長(cháng)期的技術(shù)探索與積累,攻克了高密度聲鑷換能器研發(fā)中聲場(chǎng)設計和制造工藝等難題,成功研制了二維高密度超聲換能器陣列,利用全息元素構建和時(shí)間復用的方法,結合多通道高精度時(shí)間反演超聲激勵,實(shí)現了強梯度聲場(chǎng)生成和復雜聲場(chǎng)的時(shí)空動(dòng)態(tài)調控。從生物醫學(xué)應用層面,團隊中嚴飛研究員等利用基因編輯技術(shù),在細菌細胞中產(chǎn)生了亞微米氣體囊泡,顯著(zhù)提升細菌的超聲敏感性,大幅增強其受到的聲輻射力,使得含氣囊細菌可以克服流體拉力,驅使它們在焦點(diǎn)區域聚集形成團簇(如圖3)。
當工程菌被聚集成團簇后,通過(guò)電子控制聲束沿著(zhù)預設可編程的軌跡移動(dòng),如在分叉微流腔中的細菌團簇可以選擇性地通過(guò)分叉口,或者在無(wú)邊界條件下沿著(zhù)字母A形進(jìn)行移動(dòng),或同時(shí)操控兩個(gè)團簇沿著(zhù)矩形路徑移動(dòng)。整個(gè)團簇的軌跡與預設路徑完美匹配。利用全息聲元素構架法,陣列可以產(chǎn)生具有不同拓撲電荷的聚焦渦旋。當預設的拓撲荷數發(fā)生變化時(shí),含氣囊細菌團簇所顯示的渦旋場(chǎng)模式也隨之發(fā)生變化。由于角動(dòng)量的存在,團簇可以圍繞渦旋中心連續旋轉。
生物體組織結構復雜易引起聲波畸變,且高速血流的存在也阻礙了血管內的聲操控。團隊結合相控陣全息聲鑷與顯微成像,構建動(dòng)物模型,實(shí)現了在活體動(dòng)物水平通過(guò)電子控制聲束對含氣囊工程細菌進(jìn)行可編程操控。在小鼠尾靜脈注射工程菌后,利用小鼠透明背脊皮翼視窗模型進(jìn)行觀(guān)察,打開(kāi)相控陣全息聲鑷,使得工程菌在聲束焦點(diǎn)處聚集。通過(guò)對含氣囊工程菌和普通大腸桿菌分別在小鼠背部淺表血管中進(jìn)行了聲捕獲比較,發(fā)現只有含氣囊工程菌可以被捕捉在聚焦聲束中心,并在血管中形成簇狀。進(jìn)一步,在不同直徑的血管也嘗試對含氣囊工程菌進(jìn)行了聲捕捉。隨后,通過(guò)電子偏轉聲束,實(shí)現了含氣囊工程菌的體內聲操控。在聲鑷操控下,含氣囊工程菌不僅可以沿著(zhù)血管前后移動(dòng),還可以選擇性地穿過(guò)血管分叉。也可以同時(shí)操控兩個(gè)工程菌團簇在同一條血管中,將其彼此靠近或遠離。以上研究結果表明,相控陣全息聲鑷系統操控含氣囊細菌團簇的運動(dòng)可嚴格按照程序設置進(jìn)行,展示出優(yōu)異的時(shí)空操控精度,使這些細菌能夠逆流或按需流動(dòng)到活小鼠的預設血管中。
進(jìn)一步,高通量相控陣全息聲鑷操控技術(shù)可以顯著(zhù)提高腫瘤中工程細菌的聚集效率,并結合細菌的腫瘤殺死活性,明顯抑制了腫瘤的生長(cháng)速度,延長(cháng)了荷瘤小鼠的生存期(如圖4)。
總之,本研究證明了相控陣全息聲鑷儀器系統可以作為一種活體內非接觸精準操控細胞的新工具。以相控陣全息聲鑷為手段,功能細胞及細胞球為載體,有望在免疫細胞治療,組織工程,靶向給藥等方面具有重大的應用前景。該研究工作得到了科技部重點(diǎn)研發(fā)計劃項目、國家自然科學(xué)基金、中科院和深圳市科創(chuàng )委等科技項目的資助。
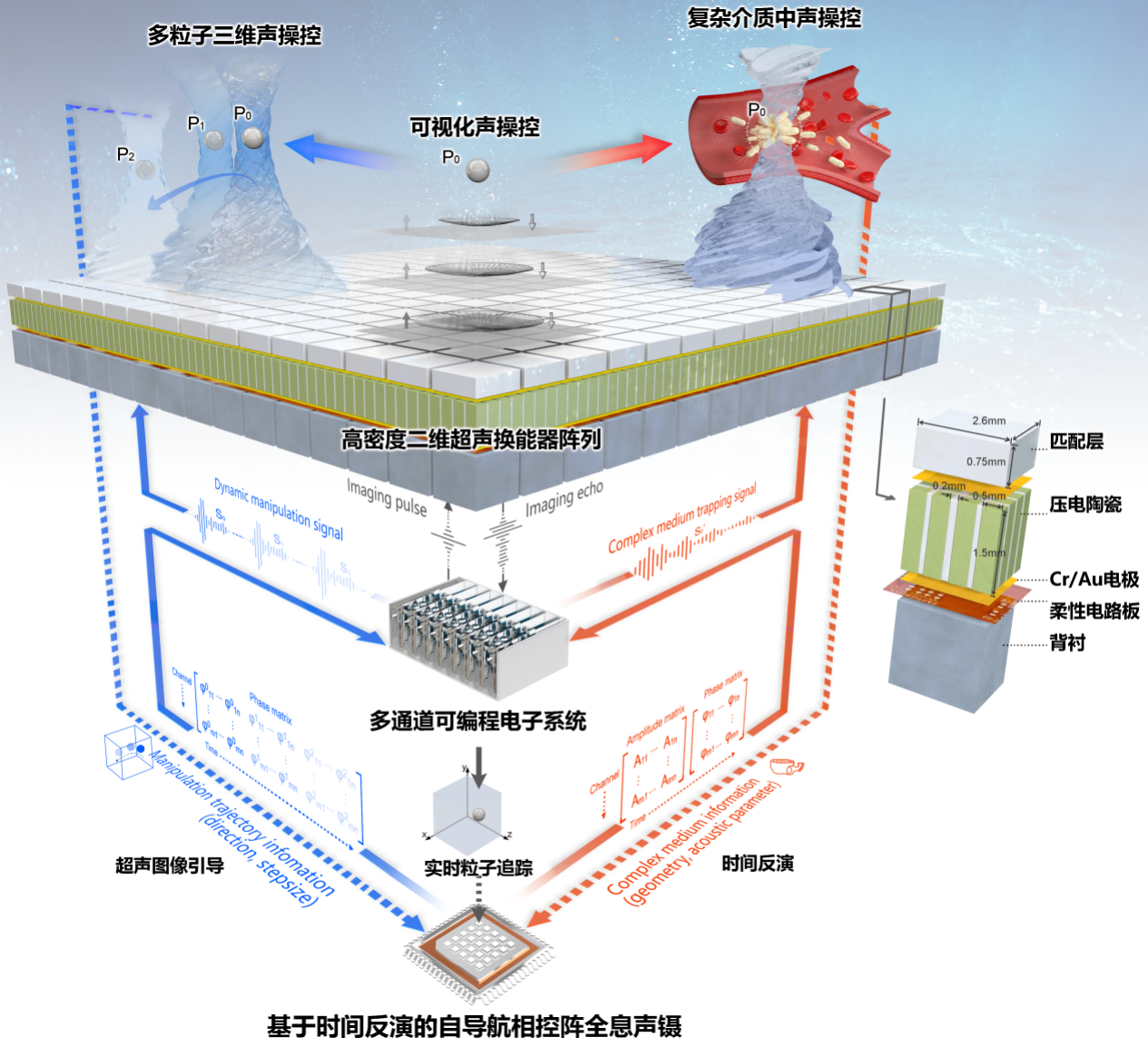
圖1 相控陣全息聲鑷系統示意圖(Research,2021)

圖2 相控陣全息聲鑷系統在體操控細胞示意圖(Nature Communications,2023)
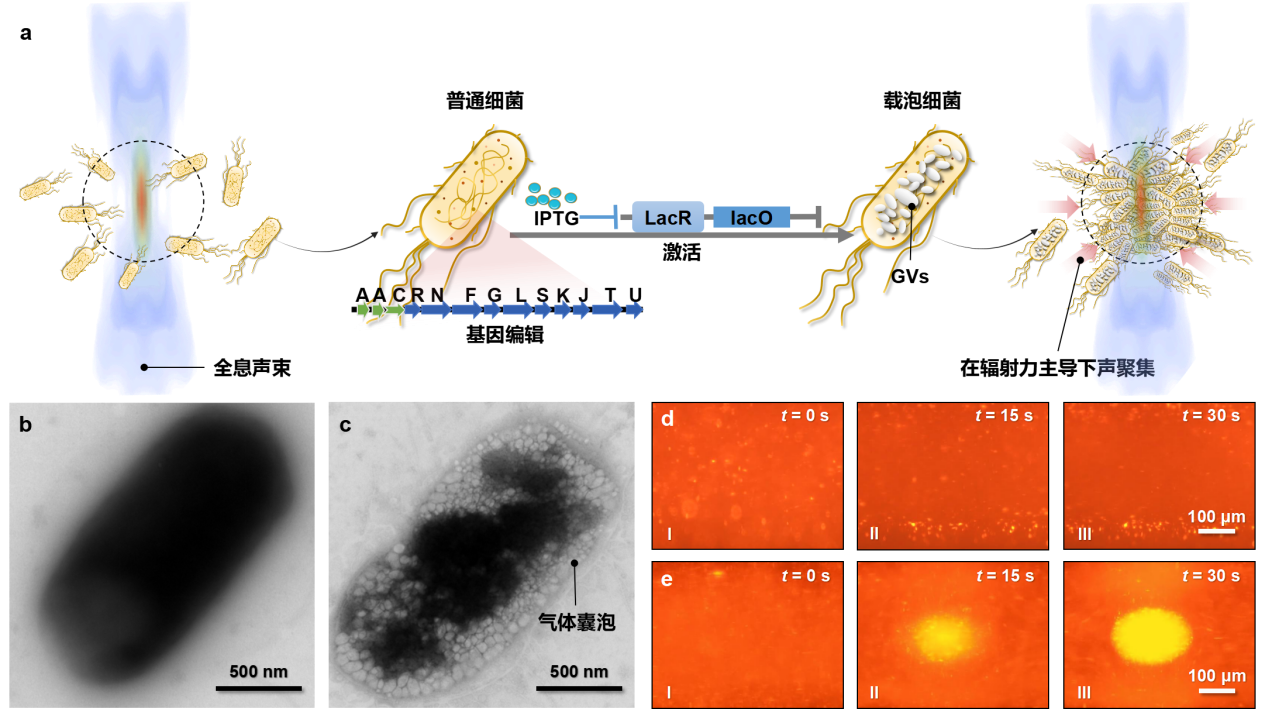
圖3 聲聚集基因編輯細菌和普通細菌對比
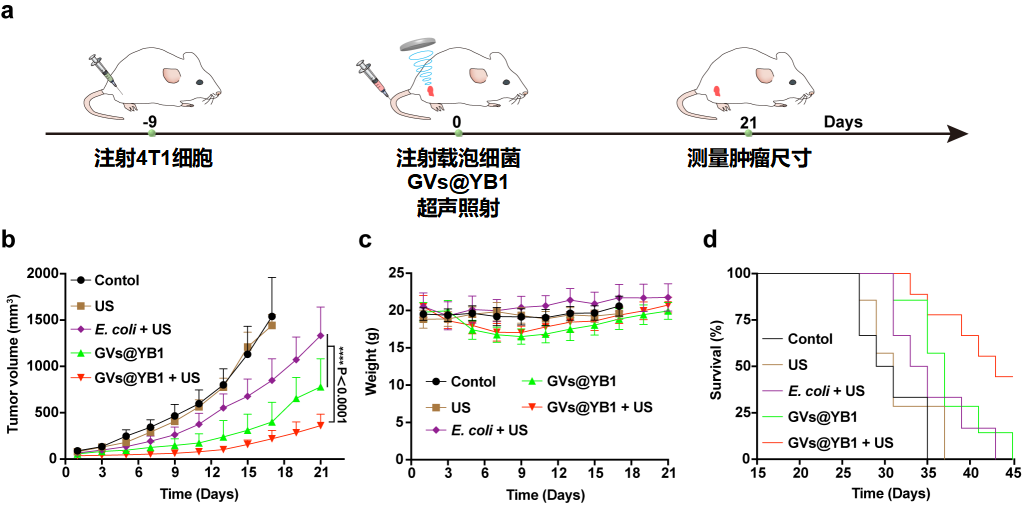
圖4 聲操控基因編輯細菌治療腫瘤實(shí)驗
附件下載:


